
質量守恆定律是什麼?國二理化必考觀念+常見陷阱解析
在國二理化中,「質量守恆定律」幾乎是每年都會考的核心觀念。 很多學生都知道一句話:反應前多重,反應後就多重。 但只要題目稍微變化,例如「燃燒後變輕」或「反應後變重」,就很容易選錯。
問題通常不在公式,而在理解不夠完整。只記結論,遇到情境變化就會失去判斷依據。
質量守恆定律不是記一句話,而是要理解「為什麼一定守恆」。
一、質量守恆定律的核心:原子只是重新排列
質量守恆定律由拉瓦節提出,內容是:在化學反應前後,總質量保持不變。
關鍵在於「微觀角度」。化學反應並不是物質消失或產生,而是原子的重新排列。
可以把它想成積木重組:把原本的形狀拆開,再拼成新的形狀。 零件的數量與種類沒有改變,所以總重量自然維持不變。
- 原子種類不變
- 原子數量不變
- 原子本身質量不變
因此,不論反應怎麼進行,總質量一定守恆。
如果想了解拉瓦節如何驗證這個定律,可以參考 維基百科:質量守恆定律。
二、為什麼秤起來會變輕或變重?關鍵在氣體
考試最常設計的陷阱,就是讓學生誤以為質量沒有守恆。 其實問題通常出在「是否把氣體算進去」。
常見情境整理:
- 密閉容器:氣體不會逸散 → 質量不變
- 開放容器(產生氣體):氣體跑掉 → 看起來變輕
- 開放容器(吸收氣體):吸收空氣 → 看起來變重
只要是化學反應,質量一定守恆。差異只是秤重時有沒有把氣體算進去。
三、計算題重點:質量與莫耳數的轉換
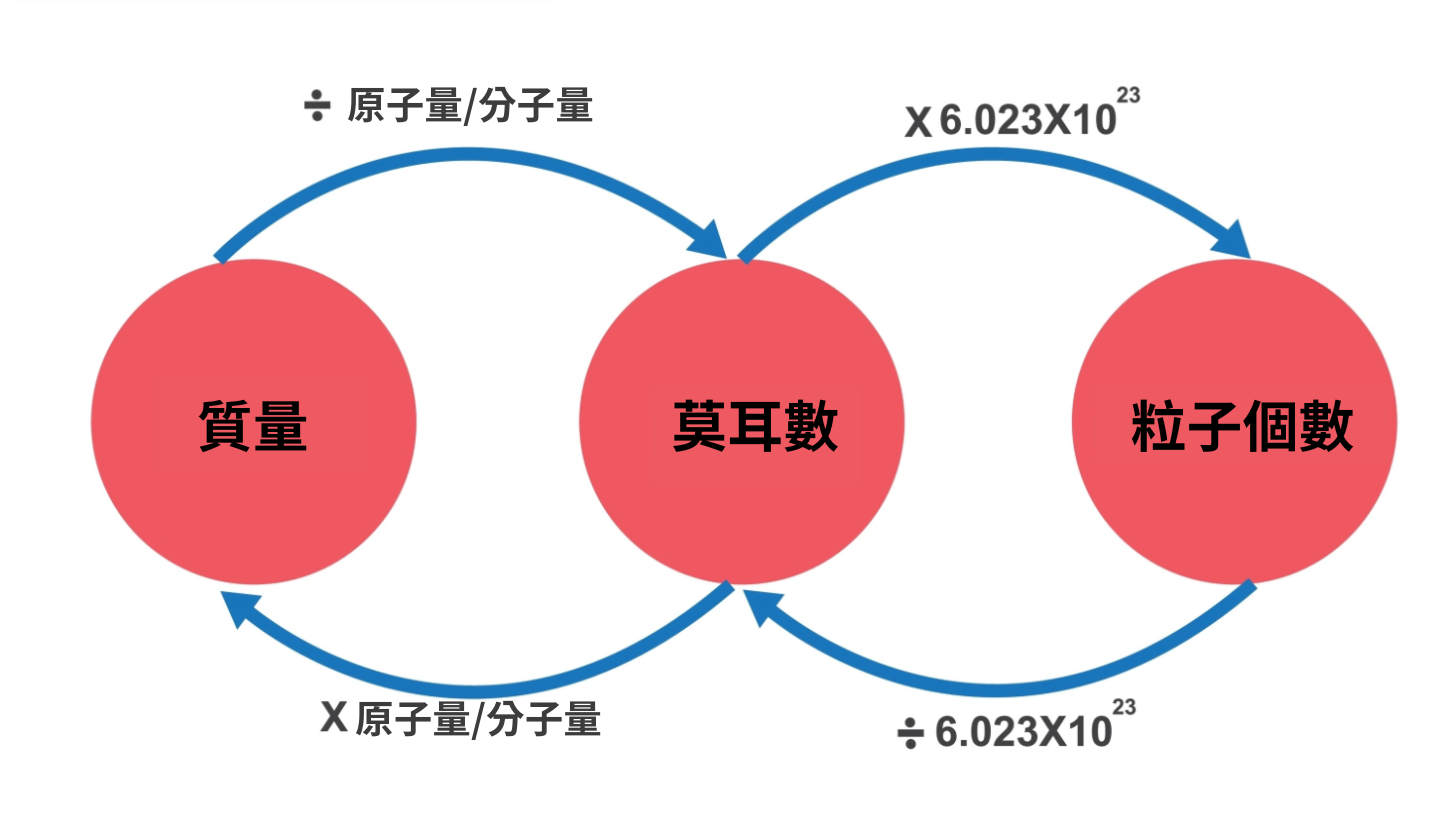
在後續單元中,質量守恆會結合莫耳數一起考,這時就不能只靠直覺判斷。
- 反應式係數代表莫耳數比例
- 不能直接當作質量比例
基本解題流程為:
- 先將已知質量換算成莫耳數
- 利用反應式比例推導另一物質莫耳數
- 再換回質量
這一類題目錯誤的原因,多半不是計算,而是觀念沒有建立完整。
結語:理解原子變化,才不會被題目誤導
質量守恆定律本身不難,但考試會透過情境變化讓學生誤判。 如果只記表面結論,很容易在變形題中失分。
當能從原子層級理解反應過程,就能在任何題型下做出正確判斷。
如果想把理化觀念建立得更穩,可以延伸閱讀 國二理化怎麼讀, 了解常見卡關點與學習方法。
